营口GMP无尘车间洁净度原因及改造措施
admin 2020-07-25 22:18:12 6692阅读
我国医药行业的《药品生产质量管理规范》(GMP)自从1992年颁布以来,已经逐步为药品生产企业所认识,接受并实施。洁净手术室按不同专科,手术间又可分为普外、骨科、妇产科、脑外科、心胸外科、泌尿外科。烧伤科、五官科等手术间。由于各专科的手术往往需要配置专门的设备及器械,因此,专科手术的手术间宜相对固定。无菌手术室室高效安全的手术室空气净化系统,保证手术室的无菌环境,可以满足器官移植、心脏、血管、人工关节置换等手术所需的高度无菌环境。采用高效低毒消毒剂,以及合理使用,是保障一般手术室无菌环境的有力措施。层流手术室手术室是采用空气洁净技术对微生物污染采取程度不同的控制,达到控制空间环境中空气洁净度适于各类手术之要求;并提供适宜的温、湿度,创造一个洁净舒适的手术空间环境。由于手术室要严格控制低细菌数及低麻醉气体浓度,所以层流超净装置的稳定性是层流净化手术室的重要验收指标。尤其是在2001年,国家药品监督管理局将制药企业完成GMP认证时间提前至2004年6月30,GMP对于企业是一项国家强制执行的政策,限期达不到要求的企业将停产。
GMP认证的核心内容是药品生产质量的全面管理和控制。其内容分为软件管理和硬件设施两部分。清洁工厂的硬件设施是最大的资本投资之一。清洁装置建成后,是否能达到设计目的,是否符合GMP要求,应通过测试来确定。在清洁车间的检测过程中,有的不符合标准,有的是局部的,也有整个项目的。如果测试不合格,尽管甲方和乙方经过整改、调试、清谷等。最后,它满足了要求,但往往会浪费大量的人力和物力,延迟施工周期,延迟GMP认证过程。在检测之前,可以完全避免一些原因和缺陷。在我们的测试工作中,我们发现不合格清洁的主要原因是:
1.工程设计不合理
这种现象比较少见,主要是在净化室水平不高的小型洁净室的建设中。现在,净化的竞争非常激烈。一些建筑单位在招标中给出了较低的报价以获得该项目。在后期施工中,使用一些不是很了解的单位,偷工减料,并使用功率较低的空调通风压缩机组,使供电和净化区域不匹配,造成不合格的清洁度。另一个原因是使用单元在设计和施工开始后增加了新的要求和清洁区域,这也将使原始设计无法满足要求。这种先天性缺陷很难改善,在工程设计阶段应该避免。作者还发现,当施工单位进行检查时,一些供气口被提前堵住,以便通过海关。
2.以低档产品取代高端产品
在洁净室中应用高效过滤器时,国家规定洁净度为100,000或更高的空气净化处理应使用初级,中级和高效过滤器的三级过滤。在验证过程中,作者发现大规模净化项目在10,000级净化水平下使用了亚高效空气过滤器而不是高效空气过滤器,导致清洁度不合格。 HEPA过滤器的最终更换符合GMP认证的要求。
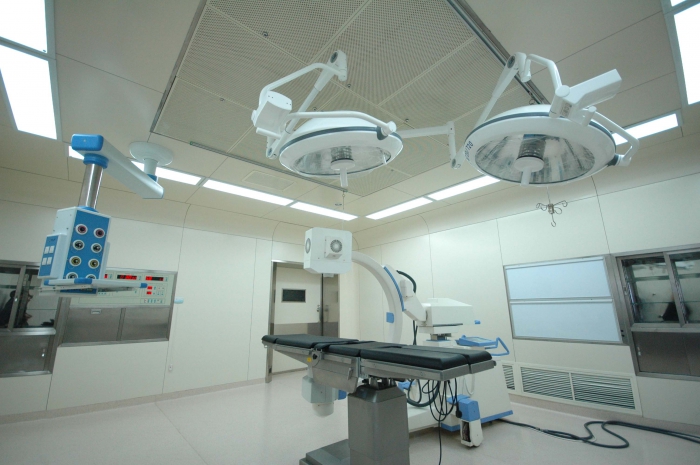
洁净室
三。供气管或过滤器密封不良。
这种现象是由粗糙的结构造成的。它将在验收期间在同一系统中显示某个房间或部分故障。改进的方法是使用漏光测试方法来检测空气供应管的泄漏,并且过滤器使用颗粒计数器来过滤过滤器。扫描部分,密封剂和安装框架以找到泄漏位置并小心密封。

 化学实验室装修设计施工哪些方面值得注意
化学实验室装修设计施工哪些方面值得注意 营口化学实验室设计装修注意要素
营口化学实验室设计装修注意要素